Sin óvulos, esperma ni útero: llega la revolución en la reproducción
Un equipo israelí ha conseguido crear embriones sintéticos de ratón que se han desarrollado hasta el día 8 de gestación
Este nuevo enfoque podría servir para estudiar los orígenes de la vida o para crear nuevos órganos para trasplantes

La investigación en torno a nuevas formas de reproducción ha vivido muchos avances en los últimos tiempos: desde la oveja Dolly a ratonas que tienen crías sin necesidad de semen, pasando por nanorobots que dirigen los espermatozoides hacia el óvulo. El último hallazgo ... ha copado titulares de todo el mundo: embriones sintéticos de ratón creados sin esperma ni óvulos, todo a partir de una suerte de 'útero artificial' y células madre cultivadas en una placa de Petri. El experimento, publicado en la revista 'Cell' y elaborado por el Instituto de Ciencias Weizmann, se plantea como toda una revolución en su campo, si bien ya existen varios laboratorios investigando esta nueva línea de desarrollo. Los más prudentes aseguran que este método marcará un antes y un después para estudiar los primeros momentos de la vida, o a comprender mejor cómo ciertas mutaciones impulsan diversas enfermedades del desarrollo; los más optimistas lo ven como una puerta para crear 'fotocopias' de nuestros órganos para cuando los originales no funcionen, e incluso para ayudar a combatir la infertilidad. En todo caso, se abre un debate ético en torno a la posibilidad de crear vida casi de la nada, abriéndose paso, como siempre, pero de una forma única y sintética.
La fórmula que permite la reproducción en mamíferos consta de varios ingredientes: un espermatozoide fecunda un óvulo, que crea una especie de 'saco' de ADN compartido que necesita de un útero que le proporcione los nutrientes necesarios para crecer. Esta es la receta tradicional. Sin embargo, ahora, el equipo israelí de Weizmann, liderado por el reconocido genetista Jacob Hanna, ha prescindido de toda esa base, creando embriones sintéticos que, vistos al microscopio, son en un 95% similares a embriones naturales y que pudieron sobrevivir hasta 8,5 días fuera de un útero. Para ello, utilizaron un biorreactor especialmente diseñado que sirve como matriz artificial para el desarrollo de embriones, una suerte de 'útero artificial' donde los embriones flotan en pequeños botes con una solución llena de nutrientes. Los vasos de precipitados están encerrados en un cilindro giratorio que los mantiene en constante movimiento y simula cómo la sangre y los nutrientes fluyen hacia la placenta. El dispositivo también replica la presión atmosférica del útero de un ratón.
Ciencia previa
No era la primera vez que se utilizaba este dispositivo: los investigadores llevaron a cabo otro experimento que fue publicado en 'Nature' en 2021 en el que el equipo consiguió cultivar embriones naturales hasta el día 11 de gestación (en total, el embarazo de una ratona es de unos 20 días). «Con eso demostramos que los embriones de mamíferos pueden crecer fuera del útero y que este órgano funciona como apoyo nutricional», explica Hanna. Este éxito les hizo dar un paso más allá y pensar en un nuevo experimento: crear embriones a partir de células madre y hacerlos crecer en su 'útero mecánico'. Para ello, extrajeron células embrionarias del ratón, capaces de convertirse en cualquier tipo de célula, y las indujeron para formar, por un lado, órganos y tejidos; por otro, la placenta; y, por último, el saco vitelino. «Los dos últimos grupos eran necesarios para crear los tejidos extraembrionarios que impulsan el desarrollo del embrión», explica Hanna en un comunicado.
El primer día, las células se unieron para formar grupos compactos que fueron introducidos en la máquina que simula el útero. Los resultados sorprendieron a todo el equipo: el día 3 de gestación los embriones comenzaron a alargarse, convirtiéndose de esferas a cilindros; tres días más tarde, el tubo neuronal empezó a plegarse en un extremo, y en el opuesto se podía observar algo que después sería la típica cola de ratón. Para el día 8, un corazón que palpitaba con normalidad comenzó a hacer circular sangre a través de los vasos que se formaron alrededor del saco vitelino del embrión. Todo de la misma forma en que la naturaleza habría hecho florecer el principio de un nuevo ser, pero sin necesidad de óvulo, esperma ni útero, solo a partir de células embrionarias de ratón, durante 8,5 días, lo que sería equivalente a un embarazo humano de aproximadamente mes y medio.

Creando ratones sin
esperma, óvulos ni útero
1
3
Los científicos obtuvieron células madre de embriones
de ratón
En el laboratorio, se empiezan a formar grupos celulares
2
Estas células, con capacidad para convertirse en cualquier tejido, se diferenciaron en células para crear:
Órganos
Placenta
La masa celular se introduce en un útero artificial
Saco vitelino
4
Esta máquina empieza a dar forma al embrión gracias al movimiento que simula la circulación de la sangre y los nutrientes
5
DÍA 3
El embrión pasa de tener una forma circular a una cilíndrica
DÍA 6
Surge el tubo neural
DÍA 7
Se crea lo que será la cola y la cabeza
DÍA 8
Tiene un corazón que bombea la sangre por todo el sistema circulatorio
Fuente: Cell / ABC
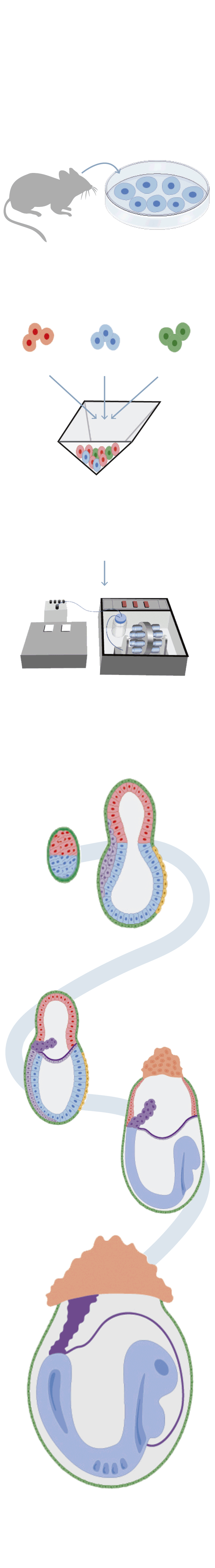
Creando ratones
sin esperma,
óvulos ni útero
1
Los científicos obtuvieron células madre de embriones de ratón
2
Estas células, con capacidad para convertirse en cualquier tejido, se diferenciaron en células para crear:
Órganos
Placenta
Saco vitelino
3
En el laboratorio, se empiezan a formar grupos celulares
La masa celular se introduce en un útero artificial
4
Esta máquina empieza a dar forma al embrión gracias al movimiento que simula la circulación de la sangre y los nutrientes
5
DÍA 3
El embrión pasa de tener una forma circular a una cilíndrica
DÍA 6
Surge el tubo neural
DÍA 7
Se crea lo que será la cola y la cabeza
DÍA 8
Tiene un corazón que bombea la sangre por todo el sistema circulatorio
Fuente: Cell / ABC
Hanna no es el único pionero. Su compañera y 'rival', Magdalena Zernicka-Goetz, de la Universidad de Cambridge, está siguiendo de forma paralela la misma línea desde hace una década. Su equipo publicará en breve dos estudios: uno con un enfoque similar al del grupo israelí («si bien hemos conseguido que nuestras estructuras en el embrión se desarrollen un poco más», explica a ABC); y un segundo, más en ciernes, en el que utilizan unas células embrionarias diferentes (células madre trofoblásticas, que se recolectan de la placenta de la ratona), con las que consiguen un mayor porcentaje de éxito y donde observan que la placenta sintética es mucho más parecida a la natural.
«Es necesario señalar que, aunque estas estructuras parecen y muestran los patrones de expresión génica de los embriones, no son embriones reales», afirma Zernicka-Goetz. El 'patrón oro' para estos embriones, según explica la investigadora, sería poder implantarlos en un útero y desarrollarse más. «Pero carecen de las estructuras necesarias para ello, como por ejemplo un cordón umbilical que le conecte con la madre», explica la investigadora. «Estos embriones han pasado la fase en la que se crean estas estructuras que los conectan con el útero, por lo que de momento es imposible que lleguen a término de manera natural», apostilla por su parte Lluis Montoliu investigador del Centro Nacional de Biotecnología del CSIC (CNB-CSIC), quien no es integrante de ninguno de estos equipos, si bien es un experto en genética reconocido mundialmente. «Son grupos de células a las que se les ha 'forzado' a cooperar entre ellas, y el resultado es esta organización en un embrión sintético. Aún así, es necesario tener en cuenta que tan solo un pequeño porcentaje de todos estos grupos ha conseguido llegar a término», señala el investigador español en referencia a que solo 50 de los 10.000 grupos celulares (un 0,5% del total) que se crearon llegaron a conformar un embrión viable hasta algo más de ocho días de desarrollo en el caso de los experimentos de Hanna, un porcentaje que sube hasta el 10% en el caso de Zernicka-Goetz. «Es una línea experimental en ciernes muy prometedora, pero aún queda mucha investigación por delante», incide Montoliu.
Aplicaciones humanas
Hanna ha fundado su propia empresa, Renewal Bio, para continuar con sus experimentos y llevarlos un paso más allá. Basándose en la idea del Nobel de Medicina, Shinya Yamanaka, que demostró que bastaba con insertar cuatro genes para transformar una célula adulta (normalmente extraída de la médula ósea o de la piel) en otra que se comportara como si fuera embrionaria (llamada célula IPS), la idea ahora es probar con sus propias células de la sangre y la piel para ver si es posible aplicar este método con humanos.
«El embrión es la mejor bioimpresora 3D. El mejor método para crear órganos y tejidos adecuados», afirma Hanna, cuya empresa ya apunta a la potencialidad del sistema para cultivar órganos a partir de las células de una persona y trasplantárselos a sí misma en el caso de que fuera necesario. Es más, en la página web de la compañía afirman que pueden «renovar la salud humana» y que su objetivo es «hacer que la humanidad sea más joven y saludable, aprovechando el poder de la tecnología con células madre», que se puede «aplicar a una amplia variedad de dolencias humanas, incluidas la infertilidad, las enfermedades genéticas y la longevidad».
MÁS INFORMACIÓN
Montoliu es crítico con estas afirmaciones: «De momento solo están estos resultados, que pueden ser muy útiles y prometedores. Pero, a partir de ahí, es especular. Queda mucho camino que recorrer». Por su parte, Zernicka-Goetz también es más conservadora que Hanna. «Nos permitirá estudiar el desarrollo de los mamíferos sin depender de embriones naturales, ya que, actualmente, para recuperarlos del útero hay que hacer una gran cantidad de disecciones en hembras». Más allá de elucubraciones, toda la comunidad científica está de acuerdo en que el estudio del grupo israelí ha dado un nuevo paso hacia un nuevo futuro en la reproducción. Ahora toca aguardar para ver a dónde nos dirige este nuevo camino.
Esta funcionalidad es sólo para suscriptores
Suscribete
Esta funcionalidad es sólo para suscriptores
Suscribete